|
RIMEMBRANZE ATOMICHE
 Ancora
una volta il collega Per. Ind. Cav. Uff. Francesco Del Bosco - nonostante
i suoi 92 anni - non cessa di stupirci. Con la sua attività e
lucidità intellettuale egli si è cimentato su un tema
scottante come "il nucleare" che pian piano sta tornando all'attenzione
degli Italiani. Il suo messaggio e la sua posizione al riguardo del
nucleare, Del Bosco - da tecnico e uomo di cultura scientifica - ce
li fa avere con queste sue rimembranze in forma di cronologia, che esprimono
il suo intatto culto per la scienza, la storia ed il progresso dell'uomo.
Il 17 di febbraio 2005, l'Enel, alla presenza del Ministro degli Esteri
italiano G. Fini, ha firmato a Bratislava l'accordo per l'acquisto del
66% delle azioni della Società elettrica slovacca Slovenskè
Electràrne, che detiene impianti nucleari. Si tratta di una riapertura
del nostro Paese verso la tecnologia nucleare oppure è soltanto
una sporadica questione di "affari"? Tra le polemiche che
un simile interrogativo ha suscitato, credo che il miglior modo per
salutare comunque questo evento e ringraziare coloro che l'hanno consentito,
sia quello di dare spazio alle "Rimembranze Atomiche" del
Cav. Uff. Del Bosco, affinché, in un clima di crisi, tensioni
geopolitiche ed instabilità economica, si possa riflettere sul
passato per meglio comprendere le più opportune vie per il futuro. Ancora
una volta il collega Per. Ind. Cav. Uff. Francesco Del Bosco - nonostante
i suoi 92 anni - non cessa di stupirci. Con la sua attività e
lucidità intellettuale egli si è cimentato su un tema
scottante come "il nucleare" che pian piano sta tornando all'attenzione
degli Italiani. Il suo messaggio e la sua posizione al riguardo del
nucleare, Del Bosco - da tecnico e uomo di cultura scientifica - ce
li fa avere con queste sue rimembranze in forma di cronologia, che esprimono
il suo intatto culto per la scienza, la storia ed il progresso dell'uomo.
Il 17 di febbraio 2005, l'Enel, alla presenza del Ministro degli Esteri
italiano G. Fini, ha firmato a Bratislava l'accordo per l'acquisto del
66% delle azioni della Società elettrica slovacca Slovenskè
Electràrne, che detiene impianti nucleari. Si tratta di una riapertura
del nostro Paese verso la tecnologia nucleare oppure è soltanto
una sporadica questione di "affari"? Tra le polemiche che
un simile interrogativo ha suscitato, credo che il miglior modo per
salutare comunque questo evento e ringraziare coloro che l'hanno consentito,
sia quello di dare spazio alle "Rimembranze Atomiche" del
Cav. Uff. Del Bosco, affinché, in un clima di crisi, tensioni
geopolitiche ed instabilità economica, si possa riflettere sul
passato per meglio comprendere le più opportune vie per il futuro.
Nel
mese di settembre 1937 i giornali pubblicavano la notizia che al fisico
italiano Enrico Fermi veniva conferito il Premio Nobel per la fisica,
precisamente per i suoi studi sui neutroni recentemente scoperti.
Quella notizia risvegliava in me i sogni infantili, quan¬do, nella
mia ignoranza. cercavo di capire cosa fossero le cose che vedevo, toccavo,
sentivo: pesanti, calde, fredde, diverse fra loro ma per me tutte uguali.
Tutto per me era misterioso. Sapevo che nel 40 a.C. un filosofo greco
aveva detto che tutte le cose erano composte da infinità di cose
tanto piccole da essere indivisibili che lui chiamò "atomi",
definizione conservata per sempre. Si sapeva che l'atomo era composto
da un nucleo pesantissimo chiamato "protone"; intorno all'ovale
giravano a grande velocità entità leggerissime, chiamate
"elettroni". che occupano lo spazio circostante. La scoperta
di Fermi risvegliava i miei sogni infantili e mi spingeva verso la ricerca
atomica, come amatore e autodidatta, limitata alle mie possibilità
di tempo, consentite dal lavoro. Oggi, 25 novembre 2004, sono passati
due terzi della mia vita e tenterò di riassumere quanto riuscirò
a ricordare.
(Cronologia
dei) ricordi sull'energia nucleare
440 a.C.
- Democrito, filosofo greco, riprende gli studi di Leucippo, afferma
che continuando a dividere un corpo si arriverà al punto che
sarà infinitamente piccolo e non più divisibile, che chiama
atomo, definizione che resterà nella storia.
1662 - Boyle scopre che l'aria è comprimibile, quando è
compressa si scalda.
1699 - Guillaume costruisce un termometro ad aria per dimostrare che
l'aria scaldandosi aumenta di volume e che a 273 °C raddoppia, raffreddandosi
a 0 °C ritorna al volume iniziale.
1803 - Dalton afferma che se due atomi di idrogeno si combinano con
uno di ossigeno formano una molecola di acqua.
1815 - Sempre Dalton sostiene che a condizioni standard di temperatura
e pressione in 1 cm tutti i gas contengono lo stesso numero di molecole;
nasce il concetto di "grammomolecola". Diventerà regola
base per determinare i pesi atomici. Si indica in stechiometria il Numero
di Avogadro.
1818 - Berzelius conferma la Regola di Avogadro e compila una tavola
dei pesi atomici.
1845 - Faraday riesce a liquefare diversi gas; quelli che non riesce
li chiama gas rari.
1852 - Frankland sostiene che gli atomi, anche diversi, si legano fra
loro secondo regole fisse per formare le molecole e le chiama "valenze".
1858 - Couper e Kekulé scoprono che il carbonio si lega con l'idrogeno
formando molecole lunghissime e le chiama "aromatiche". Indicano
le valenze con dei trattini.
1860 - Cannizzaro dimostra che con la Formula di Avogadro si possono
determinare tutti i pesi atomici e molecolari.
1869 - Mendeleev cerca di elencare gli elementi naturali secondo un
certo ordine compilando una tabella a quadri, ognuno per elemento, disponendoli
secondo i loro pesi atomici, dividendoli in periodi: il primo con 7
elementi, l'ultimo con 17. Lui stesso si accorse che non andava e la
modifica.
1870 - Mendeleev studia una nuova tabella divisa in quadretti che numera
progressivamente fino al n. 57. Nel quadro 57 raggruppa gli elementi
fino al n. 71, che chiama "terre rare": nella realtà
si scoprirà che sono metalli. Dal n. 72 al 92 continua la numerazione
progressiva: i numeri corrisponderanno al numero dei protoni o degli
elettroni componenti gli atomi e per sempre ai numeri atomici che li
distingueranno. Nel quadro ci sono alcune caselle bianche, solo numerate,
destinate a quei metalli che Mendeleev non conosceva.
La tabella 1 è composta da 7 periodi che si chiudono sempre con
un gas raro, precisamente:
 |
 |
I.
Con solo idrogeno, il più semplice e leggero, e elio - gas raro.
Il. Con 8 elementi: dal 3 al 10 chiuso col neon - gas raro.
III. Cari 8 elementi: dall'11 al 18 chiuso dall'argon - gas raro.
IV Con 18 elementi: dal 19 al 36 chiuso dal cripton - gas raro.
V. Con 18 elementi: dal 37 al 54 chiuso dal xeno - gas raro.
VI. Con 32 elementi: dal 55 all'86 chiuso dal radom - gas raro.
VII. Dall'87 francio al 92 uranio, ultimo elemento naturale.
Seguiranno con numeri progressivi tutti gli elementi artificiali scoperti
in seguito (fig. 1).
Raggi Alfa-Beta-Gamma: questi raggi sono emessi da certi elementi radioattivi.
Alfa: nuclei di elio, sono lenti, pesanti, con vita breve. Beta: sono
elettroni molto veloci, da 0,30 a 0,96 volte la velocità della
luce. La loro durata è molto lunga e certe volte sono pericolosi.
Gamma: sono onde elettromagnetiche, cortissime, molto veloci, ricche
di energia, con vita lunghissima e molto pericolose.
1895 - Roentgen utilizzando dei tubi catodici scopre i raggi che chiama
"X", molto utili in medicina. 1897 - Thomson dimostra che
ie particelle nel tubi catodici sono cariche di elettricità negativa
e le chiama "elettroni".
1897 - La studiosa polacca Maria Sklodowska, moglie del fisico Curie,
scopre il primo radioattivo naturale che chiama "radium".
Per questo viene insignita del Premio Nobel.
1897 - Thomson scopre che rinforzando raggi X con una carica elettrica
ottiene elettroni molto più potenti.
1901 - Curie scopre che un grammo di radium emette 140 calorie ogni
ora e calcola che dopo 1400 anni si riduce a metà.
1902 - Rutherford scopre che uranio e lodo sono radioattivi e con le
radiazioni genera strutture più leggere fino al piombo.
1904 - Thomson scopre che il protone ha carica elettrica positiva.
1905 - Einstein afferma che la massa di ogni corpo moltiplicata per
ia velocità della luce (i 300.000 km al secondo) al quadrato
diventa energia e stabilisce la formula
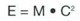
1906 - Rutherford scopre che i raggi alfa sono nuclei di elio.
1907 - Boltwood scopre che il piombo è il residuo della degradazione
dell'uranio nel corso dei tempo.
1910
- Claude scopre che un tubo pieno di gas neon emette la luce.
1911 - Rutherford suppone che il nucleo dell'atomo sia composto da protoni,
che sia pesantissimo e molto piccolo.
1911 - Millikan scopre che l'elettrone è mille volte più
leggero dell'atomo.
1913 - Rutherford sostiene che l'idrogeno è un atomo col nucleo
composto da un solo protone con carica elettrica positiva e con una
massa (peso) = 1, intorno al quale, ad una certa distanza, gira un solo
elettrone con velocità altissima, carica elettrica negativa e
con peso pressoché nullo.
1913 - Rutherford conferma che il nucleo dell'atomo ha una massa che
è pari alla somma dei protoni, che sono di numero pari al numero
atomico; a ogni protone corrisponde un elettrone con peso di 1836, 11
volte meno che viene considerato zero. In precedenza Einstein aveva
calcolato che il diametro di un atomo era di 1 cm/100.000.000, e che
il nucleo con tutto il suo peso era 10.000 volte più piccolo.
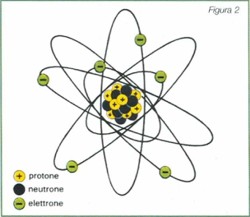
Secondo Rutherford il vuoto era occupato dalle orbite ellittiche degli
elettroni che seguivano regole precise e costanti anche nel numero dei
componenti, che secondo i periodi variano da 2-6-10-14, come si vede
chiaramente nella figura 2. L'orbita più esterna è composta
da 1 a 6 elettroni che determinano le valenze. Quando sono 6, il ciclo
si chiude e forma un gas raro che chiude anche il periodo.
1914 - Geiger inventa il contatore di particelle col suo nome.
1914 - Moseley servendosi del Metodo Avogadro controlla con precisione
diversi atomi e trova che so-no almeno il doppio del numero dei loro
protoni senza trovare la ragione.

1920
- Villard scopre un raggio molto più potente dei Raggi Alfa e
Beta, è più veloce e carico di energia, con lunga durata
e pericoloso.
1920 - Fridrik scopre il gas naturale che chiama radon - gas raro.
1920 - Richardson conferma le previsioni di Edison: i metalli caldi
emettono elettroni veloci.
1920 - Gomberg prova a legare l'atomo di carbonio con 4 valenze, con
3 atomi di idrogeno e un atomo di carbonio, formando molecole lunghissime,
composte da diversi gas del gruppo aromatico.
1926 - Schroedinger conferma la Teoria di Bohr sulle orbite degli elettroni
intorno ai nuclei.
1930 - Lawrence costruisce un ciclotrone magnetico per aumentare la
velocità dei protoni sperando di trovare altre particelle all'interno
dell'atomo.
Scoperta del neutrone
1932
- Fin da quando fu scoperto che il peso atomico del nucleo era determinato
dai protoni tutti i pesi atomici risultavano più del doppio del
loro numero. I fisici ne cercavano la ragione fino a quando Chadwick
scopriva che al protone era strettamente unita una particella senza
carica elettrica e con lo stesso peso. Questa scoperta spiegava il perché
dei pesi solo in parte. Quasi tutti i pesi atomici riportati sulle tabelle
sono numeri decimali, e creano il dubbio che nei nuclei esistano anche
neutroni, in numero maggiore dei protoni. Osservando la Tavola di Mendeleev
si nota che solo l'ossigeno, composto da 8 protoni e da 8 neutroni,
ha peso atomico pari a 16.
1932 - Chadwick conferma che il nucleo dell'atomo è composto
da protoni ai quali è strettamente unito un neutrone con lo stesso
peso, uguale a 1, come quello dell'idrogeno; scopre che nei nuclei possono
esserci anche neutroni liberi, che contribuiscono a determinare il peso
atomico, conservano lo stesso numero atomico come si vede dalla figura
1, dove i pesi atomici sono maggiori del doppio dei protoni e sono decimali,
perché vengono pesati in massa frammisti.
Secondo la figura 1, il numero dei neutroni eccedenti aumenta in rapporto
con i! loro numero atomico; infatti l'uranio 238 è composto da
92 protoni e da 146 neutroni, quindi sono 54 in più.
Solo l'ossigeno è composto da 8 protoni più 8 neutroni
= 16 (peso atomico 15,999).
0 = 16 è la base per determinare i pesi atomici.
Dimensioni
dell'atomo immaginato sferico
 Diametro esterno = 1 cm/100.000.000 = (10^-8 cm).
Diametro esterno = 1 cm/100.000.000 = (10^-8 cm).
 Diametro
del nucleo = 1 cm/1.000.000.000.000 =(10^12 cm). Diametro
del nucleo = 1 cm/1.000.000.000.000 =(10^12 cm).
Immaginando il nucleo con diametro = 1 cm avremo un diametro esterno
di 100 m: lo spazio interno è completamente occupato dado orbite
elettroniche, secondo lo schema di Bohr considerati con peso = 0.
Esperimento
di Fermi
1934
- Appena scoperti i neutroni Fermi pensa di sfruttare quelli in soprannumero
scoperti nell'uranio: prova a bombardarli con i raggi del radium ottenendo
neutroni molto veloci senza risultati, continua le prove, aiutato da
diversi colleghi, concludendo che si deve ridurre la veloeità
dei neutroni. Dopo una lunga serie di prove scopre che il migliore schermo
(rallentatore) è la grafite.
 In
seguito ad una serie di bombardamenti con i raggi del radium nella massa
trova un materiale diverso dall'uranio e spera di aver scoperto il primo
elemento artificiale. Lo pubblica su una rivista tedesca, richiamando
l'interesse degli altri fisici. tra cui il tedesco Strassman che studiava
l'acqua pesante. In
seguito ad una serie di bombardamenti con i raggi del radium nella massa
trova un materiale diverso dall'uranio e spera di aver scoperto il primo
elemento artificiale. Lo pubblica su una rivista tedesca, richiamando
l'interesse degli altri fisici. tra cui il tedesco Strassman che studiava
l'acqua pesante.
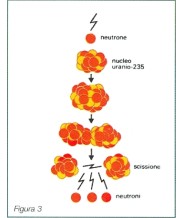
1935 - Strassman Insieme al chimico Hahn studia con interesse le comunicazioni
di Fermi e trova che non era nessun elemento nuovo, confermando che
Fermi aveva spaccato in due il nucleo dell'atomo, realizzando ia fissione
nucleare. Per questo Fermi viene proposto per il Premio Nobel e prosegue
gli studi (fig. 3).
1937 - Il collega di Fermi, Segrè, scopre l'elemento n. 43 tecnezio,
che mancava dalla Tavola di Mendeleev.
1937 - Dempster scopre che esiste un atomo di ura¬nio con peso 235
perché ha soli 143 neutroni, è rarissimo e radioattivo
e presente con meno dei 5% nel 238.
1937 - Viene assegnato a Fermi il Premio Nobel per i neutroni lenti.
1938 - Fermi si reca a Stoccolma per ritirare il Premio Nobel e parte
direttamente per gli Stati Uniti, dove insegnerà all'Università
di Chicago, continuando i suoi studi e le sue esperienze, sperando di
trovare il modo di trasformare l'energia potenziale dell'uranio in energia
cinetica. Durante le sue prove Fermi scopriva che il litio neutralizzava
i neutroni rallentando la loro velocità ed energia. Pensava che
una massa sufficiente di uranio 238 emettesse una quantità di
neutroni capaci di innescare la reazione naturale per produrre calore
e di limitare la temperatura a 500 °C introducendo le barre di litio
in fianco a quelle fisse di uranio. Mentre continuava le sue prove cercava
di accumulare il materiale che riteneva necessario. Fermi pensava che
con una massa di grafite avente una quantità di fori paralleli
contenenti le barre di uranio fisse e quelle di litio regolabili, raffreddando
tutto con acqua, si potesse provare cosa succedeva con l'emissione di
neutroni rallentati dalla grafite, che la reazione nucleare controllata
continuasse ad autoalimentarsi e che si potesse controllare col movimento
delle barre di litio. Il giorno 2 dicembre 1942 Fermi, convinto della
bontà dei suoi studi, invitava i colleghi fisici alla prova definitiva
della Reazione nucleare a catena autocontrollata. Fermi,
che nel 1942 disponeva di 6.000 kg di uranio puro U 238, sosteneva che
per avere una reazione a catena spontanea necessitasse una quantità
di uranio U 235 con una massa critica capace di emettere neutroni veloci
tanto da innescare una reazione a catena, che avrebbe provocato lentamente
la fissione di tutta la massa.
 Per
evitare il pericolo dell'esplosione considerava indispensabile il rallentamento
della velocità dei neutroni, che riteneva possibile interponendo
grafite pura. Per una prova definitiva Fermi proponeva di impilare 1200
tonnellate di grafite pura intercalate con barre di uranio puro e barre
in ossido di uranio e inoltre, per controllare l'emissione di neutroni,
introdurre barre di litio capaci di assorbire neutroni. La grafite doveva
servire a rallentare la velocità dei neutroni in modo da poterli
controllare, evitando ogni pericolo di esplosione. I neutroni lenti
avrebbero colpito i nuclei degli atomi di uranio dividendoli in due
parti e provocandone la fissione controllata. Il raffreddamento della
grafite veniva effettuato con caduta di acqua a pioggia, poi, ad un
certo punto, le prove dovevano essere sospese per evitare il pericolo
di surriscaldamento. Per
evitare il pericolo dell'esplosione considerava indispensabile il rallentamento
della velocità dei neutroni, che riteneva possibile interponendo
grafite pura. Per una prova definitiva Fermi proponeva di impilare 1200
tonnellate di grafite pura intercalate con barre di uranio puro e barre
in ossido di uranio e inoltre, per controllare l'emissione di neutroni,
introdurre barre di litio capaci di assorbire neutroni. La grafite doveva
servire a rallentare la velocità dei neutroni in modo da poterli
controllare, evitando ogni pericolo di esplosione. I neutroni lenti
avrebbero colpito i nuclei degli atomi di uranio dividendoli in due
parti e provocandone la fissione controllata. Il raffreddamento della
grafite veniva effettuato con caduta di acqua a pioggia, poi, ad un
certo punto, le prove dovevano essere sospese per evitare il pericolo
di surriscaldamento.
Per la prova di collaudo, Fermi fece sovrapporre i blocchi di grafite,
tanto da formare una pila alta più di 6 metri.
Il complesso aveva le seguenti dimensioni:
 Lunghezza
30 piedi + 3 pollici = 9,65 m Lunghezza
30 piedi + 3 pollici = 9,65 m
 Larghezza
e altezza 20 piedi + 2 pollici = 6,60 m Larghezza
e altezza 20 piedi + 2 pollici = 6,60 m
 Volume
420 m3 Volume
420 m3
 Peso
della grafite 1200 t Peso
della grafite 1200 t
 Peso
delle barre di uranio U 238 6 t Peso
delle barre di uranio U 238 6 t
 Peso
delle barre in ossido di uranio 40 t Peso
delle barre in ossido di uranio 40 t
 Peso
delle barre in litio 34 t Peso
delle barre in litio 34 t
 Peso
totale della pila 1300 t. L'esperimento definitivo venne fissato per
il giorno 2 dicembre 1942, con inizio subito al mattino. Peso
totale della pila 1300 t. L'esperimento definitivo venne fissato per
il giorno 2 dicembre 1942, con inizio subito al mattino.
Purtroppo estraendo ie barre di litio non si notò nessun segno
di emissione di neutroni, perché i contatori Geiger non davano
alcun segnale. Fermi intuì immediatamente che la massa critica
non era sufficiente e fece aggiungere altro ossido di uranio e grafite.
Finalmente, alle ore 15.45 dello stesso giorno, quando furono estratte
quasi totalmente le barre di litio, i contatori Geiger segnalarono l'emissione
di neutroni, confermando le previsioni di Fermi. Per la prima volta
l'uomo riusciva a provocare una reazione atomica a catena capace di
autosostenersi e di essere controllata; iniziava così l'era atomica.
Per comodità di linguaggio coi suoi colleghi, Fermi chiamò
il mucchio di grafite e uranio "pila" e da allora sempre,
impropriàmente, fu chiamata così. Fermi aveva trovato
il sistema di ricavare l'energia latente dall'uranio; ora era il momento
di impegnare i tecnologi a progettare le macchine adatte al futuro sviluppo.
Il ciclotrone che aveva dimostrato la sua validità nel trattamento
dei materiali fissili veniva potenziato con risultati sempre più
positivi. Si scopriva che il neutrone poteva emettere un elettrone con
carica negativa, si trasformava in protone con carica elettrica positiva,
creando un nuovo elemento artificiale con numero atomico successivo.
Trattando, al ciclotrone si possono ottenere anche sostanze radioattive
con periodi da pochi secondi fino a decine di anni; alcune emettono
Raggi Alfa, Beta e Gamma.
Dopo il disastro del 26 aprile 1986 a Cernobyl, in Italia un referendum
promosso dai Radicali richiedeva di non progettare né di costruire
altre pile termonucleari. Il risultato positivo fu inteso dal Governo
in senso estensivo; si decise di abolire totalmente ogni sfruttamento
della tecnologia nucleare e smantellare quelle centrali allora esistenti,
anche qualcuna modernissima, e trasformare a carbone quelle già
costruite al 60%.
Risultato attuale: importazione del 20% dell'elettricità
necessaria con gravissimo danno alla nostra economia.
Bibliografia
• Dati scientifici - tabelle - Riviste del CNEN (Comitato Nazionale
Energia Nucleare) 1970
• "Enciclopedia della Civiltà Atomica° - Edizione II
Saggiatore 1960
Bibliografia
Rocco Morelli
Il Perito Industriale - 03/2005
|
 Ancora
una volta il collega Per. Ind. Cav. Uff. Francesco Del Bosco - nonostante
i suoi 92 anni - non cessa di stupirci. Con la sua attività e
lucidità intellettuale egli si è cimentato su un tema
scottante come "il nucleare" che pian piano sta tornando all'attenzione
degli Italiani. Il suo messaggio e la sua posizione al riguardo del
nucleare, Del Bosco - da tecnico e uomo di cultura scientifica - ce
li fa avere con queste sue rimembranze in forma di cronologia, che esprimono
il suo intatto culto per la scienza, la storia ed il progresso dell'uomo.
Il 17 di febbraio 2005, l'Enel, alla presenza del Ministro degli Esteri
italiano G. Fini, ha firmato a Bratislava l'accordo per l'acquisto del
66% delle azioni della Società elettrica slovacca Slovenskè
Electràrne, che detiene impianti nucleari. Si tratta di una riapertura
del nostro Paese verso la tecnologia nucleare oppure è soltanto
una sporadica questione di "affari"? Tra le polemiche che
un simile interrogativo ha suscitato, credo che il miglior modo per
salutare comunque questo evento e ringraziare coloro che l'hanno consentito,
sia quello di dare spazio alle "Rimembranze Atomiche" del
Cav. Uff. Del Bosco, affinché, in un clima di crisi, tensioni
geopolitiche ed instabilità economica, si possa riflettere sul
passato per meglio comprendere le più opportune vie per il futuro.
Ancora
una volta il collega Per. Ind. Cav. Uff. Francesco Del Bosco - nonostante
i suoi 92 anni - non cessa di stupirci. Con la sua attività e
lucidità intellettuale egli si è cimentato su un tema
scottante come "il nucleare" che pian piano sta tornando all'attenzione
degli Italiani. Il suo messaggio e la sua posizione al riguardo del
nucleare, Del Bosco - da tecnico e uomo di cultura scientifica - ce
li fa avere con queste sue rimembranze in forma di cronologia, che esprimono
il suo intatto culto per la scienza, la storia ed il progresso dell'uomo.
Il 17 di febbraio 2005, l'Enel, alla presenza del Ministro degli Esteri
italiano G. Fini, ha firmato a Bratislava l'accordo per l'acquisto del
66% delle azioni della Società elettrica slovacca Slovenskè
Electràrne, che detiene impianti nucleari. Si tratta di una riapertura
del nostro Paese verso la tecnologia nucleare oppure è soltanto
una sporadica questione di "affari"? Tra le polemiche che
un simile interrogativo ha suscitato, credo che il miglior modo per
salutare comunque questo evento e ringraziare coloro che l'hanno consentito,
sia quello di dare spazio alle "Rimembranze Atomiche" del
Cav. Uff. Del Bosco, affinché, in un clima di crisi, tensioni
geopolitiche ed instabilità economica, si possa riflettere sul
passato per meglio comprendere le più opportune vie per il futuro.


 In
seguito ad una serie di bombardamenti con i raggi del radium nella massa
trova un materiale diverso dall'uranio e spera di aver scoperto il primo
elemento artificiale. Lo pubblica su una rivista tedesca, richiamando
l'interesse degli altri fisici. tra cui il tedesco Strassman che studiava
l'acqua pesante.
In
seguito ad una serie di bombardamenti con i raggi del radium nella massa
trova un materiale diverso dall'uranio e spera di aver scoperto il primo
elemento artificiale. Lo pubblica su una rivista tedesca, richiamando
l'interesse degli altri fisici. tra cui il tedesco Strassman che studiava
l'acqua pesante. Per
evitare il pericolo dell'esplosione considerava indispensabile il rallentamento
della velocità dei neutroni, che riteneva possibile interponendo
grafite pura. Per una prova definitiva Fermi proponeva di impilare 1200
tonnellate di grafite pura intercalate con barre di uranio puro e barre
in ossido di uranio e inoltre, per controllare l'emissione di neutroni,
introdurre barre di litio capaci di assorbire neutroni. La grafite doveva
servire a rallentare la velocità dei neutroni in modo da poterli
controllare, evitando ogni pericolo di esplosione. I neutroni lenti
avrebbero colpito i nuclei degli atomi di uranio dividendoli in due
parti e provocandone la fissione controllata. Il raffreddamento della
grafite veniva effettuato con caduta di acqua a pioggia, poi, ad un
certo punto, le prove dovevano essere sospese per evitare il pericolo
di surriscaldamento.
Per
evitare il pericolo dell'esplosione considerava indispensabile il rallentamento
della velocità dei neutroni, che riteneva possibile interponendo
grafite pura. Per una prova definitiva Fermi proponeva di impilare 1200
tonnellate di grafite pura intercalate con barre di uranio puro e barre
in ossido di uranio e inoltre, per controllare l'emissione di neutroni,
introdurre barre di litio capaci di assorbire neutroni. La grafite doveva
servire a rallentare la velocità dei neutroni in modo da poterli
controllare, evitando ogni pericolo di esplosione. I neutroni lenti
avrebbero colpito i nuclei degli atomi di uranio dividendoli in due
parti e provocandone la fissione controllata. Il raffreddamento della
grafite veniva effettuato con caduta di acqua a pioggia, poi, ad un
certo punto, le prove dovevano essere sospese per evitare il pericolo
di surriscaldamento.